- Un blocco di rame di massa 50 g a una temperatura di 127 °C viene posto in un contenitore isolante con un blocco di piombo di massa 10 g che ha una temperatura di -73 °C. Qual'è la temperatura di equilibrio di questo sistema costituito dai due blocchi ? Qual'è la variazione di energia interna del sistema dei due blocchi quando passa dalla condizione iniziale alla condizione di equilibrio ? Qual'è la variazione di entropia del sistema dei due blocchi ? (R: 46 °C, 0 J, +1.72 J/°K)

- Una macchina termica reversibile lavora con quattro sorgenti. Dalla prima, a temperatura T1= 227 °C, la macchina assorbe il calore Q1= 5000 J, alla quarta sorgente, a temperatura T4= 7 °C, la macchina cede il calore Q4= -1460 J. Con la seconda e terza sorgente, rispettivamente alle temperature T2= 127 °C e T3= 27 °C, la macchina scambia i calori Q2 e Q3= - Q2. Calcolare il rendimento della macchina. (R: 33%)

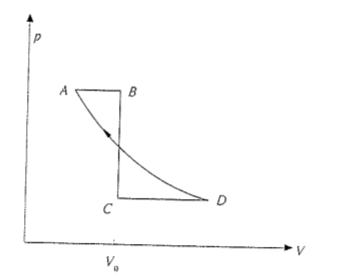
- Un gas ideale biatomico, a pressione p0= 1 atm, volume V0= 10 l e temperatura T0= 20 °C, viene compresso adiabaticamente e reversibilmente fino a V= 1.5 l. Dopo un certo tempo il gas torna alla temperatura iniziale T0 a causa dell'imperfetto isolamento termico. Calcolare la massima pressione raggiunta, la massima temperatura, la pressione finale del gas, la variazione di entropia del gas. (R: 1442400 Pa, 626 °K, 676000 Pa, -6.55 J/°K)

- Una mole di gas ideale (P0= 1 bar, V0= 30 l) assorbe reversibilmente da una sorgente T0 il calore Q= 4186 J. Calcolare il volume finale occupato dal gas. Il lavoro prodotto dal gas durante l'espansione viene interamente ceduto sotto forma di calore a una sorgente T1= 327 °C e viene poi sottratto alla sorgente da una macchina reversibile che lavora tra T1 e T0 . Calcolare il lavoro prodotto dalla macchina e la variazione di entropia dell'universo dell'intero processo. (R: 121 l, 394 J, +12.8 J/°K)

- Una macchina termica reversibile lavora tra le due sorgenti, una costituita dall'ambiente a T1= 17 °C e l'altra da una grande massa di stagno fuso alla temperatura T2 di fusione. Ad ogni ciclo della macchina solidificano 8.4 g di stagno, viene compiuto il lavoro 210 J e viene ceduto alla sorgente a T1 il calore Q1= -283 J. Calcolare il valore di T2 e da questi dati anche il calore latente di fusione dello stagno. (R: 505 °K, 58700 J/kg)

- Una macchina termica reversibile assorbe Q2 = 200 kJ da una sorgente a T2= 973 °K, cede Q1 a una sorgente a T1= 573 °K e Q3 = Q1 a una sorgente a temperatura T3 = 373 °K. Calcolare il valore di Q1, il lavoro totale, il rendimento e le variazioni di entropia di ciascuna sorgente. (R: Q1= - 46 kJ, W= 108 kJ, η= 54%, ΔS1= 81 J/°K, ΔS2= -205 J/°K, ΔS3= 124 J/°K,)

- Un contenitore adiabatico di volume 2V è diviso in due parti uguali A e B da una parete adiabatica fissa. Da entrambe le parti ci sono 3 moli di idrogeno alla temperatura di 300 °K. Con una trasformazione adiabatica reversibile il gas nelle parte A viene compresso spendendo un lavoro di -12.47 kJ. La parete adiabatica fissa non è ideale e dopo un certo tempo si stabilisce un equilibrio termico tra le parti A e B. Successivamente, con una trasformazione ancora reversibile si riporta il volume della parte A al valore iniziale. Di nuovo, dopo un certo tempo, si ristabilisce l'equilibrio termico. Determinale la temperatura finale e la variazione di entropia dell'universo nell'intero processo. (R: 320 °K , + 3.22 J/°K)

- Cinque moli di azoto sono contenute, alla temperatura di 250 °C, nel volume V di un cilindro collegato ad un altro cilindro da un rubinetto chiuso. Il secondo cilindro è vuoto e ha un volume 4V. Il gas compie nel primo cilindro un'espansione adiabatica reversibile occupando un volume 4V. Si apre poi il rubinetto e il gas riempie anche il secondo cilindro. Il sistema è termicamente isolato. Calcolare la variazione di energia interna e di entropia in ciascuna trasformazione. (R: -23134 J; 0 J/°K; 0, 28,8 J/°K)

- Un frigorifero reversibile funziona tra 25°C e -4 °C, assorbendo -400 J di lavoro in un ciclo. Vi si pone all'interno 1 kg di acqua a 20 °C. Calcolare quanti cicli deve compiere la macchina per trasformare tutta l'acqua in ghiaccio a -4 °C. (R: 115 cicli)

- Un contenitore adiabatico è diviso in due parti da un setto che conduce bene il calore; nella parte A ci sono 2 moli di gas elio (VA= 20 l), nella parte B 1 mole di idrogeno (VB= 10 l) . Il sistema è in equilibrio termico a T0= 290 °K. Con il rapido spostamento di una parete mobile nella parte A il volume VA viene ridotto a 5 l; il lavoro necessario è -12.7 kJ. Ristabilito l'equilibrio termico VA viene riportato reversibilmente al valore iniziale. Calcolare la temperatura finale del sistema e la variazione di entropia dell'universo in tutto il processo. (R: 343 °K; 7.66 J/°K)

- Un recipiente rigido adiabatico è diviso in due parti eguali, di volume 10 l ciascuna, da una parete fissa che conduce bene il calore. In una parte, A, è contenuta una mole di Neon a 300 °K, nell'altra parte, B, c'è il vuoto. All'estremità della parte B c'è un pistone che può scorrere senza attrito. Nella parete fissa viene aperto un rubinetto e il gas si espande da A fino ad occupare tutto il volume di A e B. A equilibrio raggiunto si comprime reversibilmente il gas in A in modo da svuotare la parte B e si chiude il rubinetto. Si tira indietro il pistone nella parte B L'operazione viene ripetuta due volte. Calcolare la temperatura finale. (R: 756 °K)

- Un contenitore adiabatico è diviso in due parti di egual volume, di 2 l, da una parete adiabatica fissa; da entrambi le parti pressione e temperatura hanno gli stessi valori p0= 10 atm e T0= 0 °C; nella parte destra c'è Idrogeno; nell'altra Elio. Tramite un riscaldatore elettrico viene ceduto all'idrogeno Q= 2 kJ. Successivamente l'elio viene compresso in modo adiabatico reversibile fino a che la sua pressione eguaglia quella dell'idrogeno. A seguito del non perfetto isolamento termico dopo un certo tempo i due gas raggiungono l'equilibrio termico. Calcolare la temperatura finale del sistema, la differenza di pressione finale tra le due parti, la variazione complessiva di energia interna e di entropia del sistema. (R: 355 °K; 3 atm; 2430 J; 6.1 J/°K)